CONTENIDOS: ENLACES A SECCIONES
- NOTAS INTRODUCTORIAS
- MÉTODOS CLÁSICOS DE ENFRIAMIENTO EN CRIOBIOLOGÍA
- ENFRIAMIENTO A LA TEMPERATURA DE TRANSICIÓN DEL CRISTAL
- TASA DE ENFRIAMIENTO CRÍTICO PARA VITRIFICACIÓN
- MÉTODOS DE ENFRIAMIENTO EN CRIONICA
- ESTRÉS Y TENSIÓN A BAJA TEMPERATURA
- PROTOCOLO DE ENFRIAMIENTO CERCA DE Tg PARA PACIENTES CON CRIONICS VITRIFICANTES
- ALMACENAMIENTO POR ENCIMA DE LA TEMPERATURA DEL NITRÓGENO LÍQUIDO
I. OBSERVACIONES INTRODUCTORIAS
Los problemas relacionados con el enfriamiento imponen restricciones a la práctica exitosa de la criónica . En un intento por ver estos problemas en perspectiva, he tratado de ver qué se puede aprender de la ciencia de los materiales, la ciencia de los alimentos y la criobiología con respecto a las propiedades que cambian con la temperatura, incluidos parámetros como la viscosidad, la expansión térmica, la capacidad calorífica específica, la conductividad térmica, la compresibilidad. , temperatura de transición vítrea, etc. Enfoco mi atención en el enfriamiento de un paciente criogénico que está cargado o siendo cargado con crioprotector vitrificante, pero empiezo discutiendo los métodos clásicos de enfriamiento en criobiología.
(Para obtener detalles sobre el tiempo de reutilización inicial inmediatamente después de la desanimación, consulte Preparación para emergencias para un grupo local de criónica ).
II. MÉTODOS CLÁSICOS DE ENFRIAMIENTO EN CRIOBIOLOGÍA
La criónica no es criobiología y la criobiología no es criónica. La criónica es la crioconservación de humanos y animales dañados por enfermedades, envejecimiento y el propio proceso de crioconservación con la esperanza y expectativa de que la ciencia futura podrá reparar ese daño. La criobiología es una ciencia contemporánea establecida que estudia los efectos de las bajas temperaturas en los organismos e intenta aplicar ese conocimiento a la crioconservación. Los crionicistas se benefician al aprender de los criobiólogos.
La preservación de órganos tiene la mejor oportunidad de éxito mediante el uso de la vitrificación , razón por la cual los crionicistas están tan interesados en este método de criopreservación. Pero muchos criobiólogos continúan usando métodos clásicos de crioconservación que implican la congelación porque estos métodos minimizan la toxicidad crioprotectora y pueden tener un éxito tolerable cuando se aplican a células o embriones (en lugar de tejidos u órganos). Algunos de los principios subyacentes a los métodos clásicos de criopreservación son relevantes para la vitrificación, por lo que es útil que los crionicistas los entiendan.
El agua dentro de las células vivas se puede dividir aproximadamente entre agua que es osmóticamente activa y agua que está estrechamente unida a proteínas, ADN y fosfolípidos, principalmente proteínas. Los iones también son hidratados por el agua, por lo que los iones de potasio hidratado (número atómico 19) (que tienen un diámetro hidratado de 3,8 Angstroms ) pueden pasar a través de canales iónicos más pequeños que los iones de sodio (número atómico 11) (que tienen un diámetro hidratado de 5 Angstroms). ). Si una célula se deshidrata osmóticamente por exposición a un ambiente hipertónico, la cantidad de agua que no se puede eliminar osmóticamente es aproximadamente el 10% del agua total de la célula. El hecho de que el 10% del agua celular sea agua ligada (agua "ligada" por enlaces de hidrógeno a macromoléculas) ha sido confirmado por RMN , Medida dialéctica, isotermas de adsorción y calorimetría . La calorimetría demuestra que el agua unida no muestra calor de fusión, es decir, el agua osmóticamente inactiva en una célula no se congela. El agua ligada es tan viscosa que se vitrifica a temperaturas criogénicas. Las mediciones del Calorímetro de Barrido Diferencial ( DSC ) de las células sometidas a enfriamiento también indican que alrededor del 10 % del agua de la célula es incapaz de congelarse [CRIOBIOLOGÍA; Schrenders,PD; 33(5):487-501 (1996) y CRIOBIOLOGÍA; Sol,WQ; 38(4):372-385 (1999)].
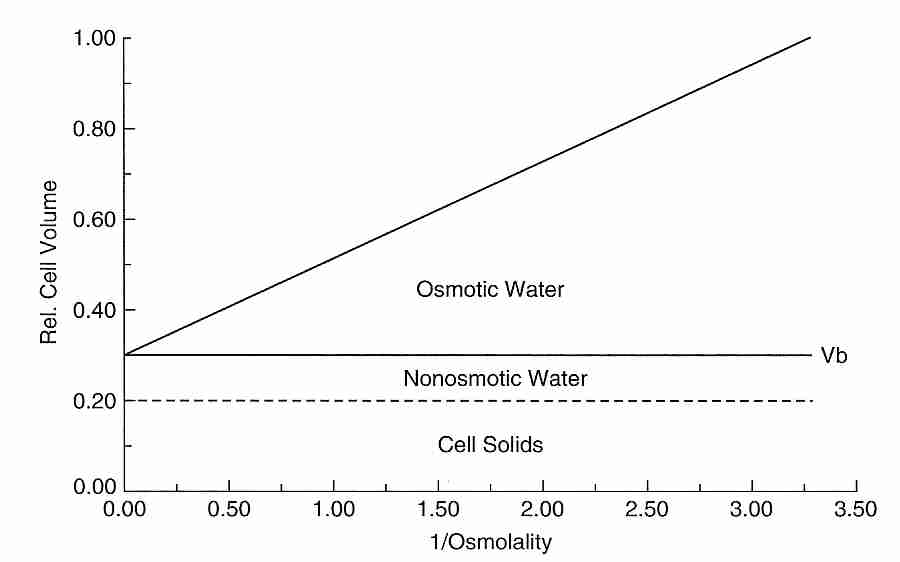 |
Los criobiólogos a menudo intentan determinar cuantitativamente el porcentaje de agua osmóticamente activa congelable en una célula y el porcentaje del volumen celular que es osmóticamente inactivo. La porción osmóticamente inactiva de la célula consta de sólidos celulares y agua ligada. Los criobiólogos suelen estimar la fracción osmóticamente inactiva de una célula mediante el uso de un diagrama de Boyle-van't Hoff , que representa gráficamente el volumen celular como variable dependiente y el recíproco de la osmolalidad externa como variable independiente. La osmolalidad es el recuento de partículas osmóticamente activas en una solución (es decir, moles de soluto por kilogramo de solución para todos los solutos en la solución). Cuanto mayor sea la osmolalidad de la solución externa, más agua saldrá osmóticamente de la célula y más se reducirá el tamaño de la célula a un volumen celular más pequeño. Una celda puede exponerse a varias osmolalidades y los volúmenes de celda resultantes pueden medirse. Cuando estos valores se colocan en un diagrama de Boyle-van't Hoff, deben estar aproximadamente en línea recta (la ecuación de Boyle-van't Hoff) porque la relación entre el volumen celular y la osmolalidad externa es lineal cuando la osmolalidad no es demasiado baja. Extrapolando la línea al eje vertical se obtiene el volumen celular osmóticamente inactivo, correspondiente a una osmolalidad externa infinita y una célula que se ha encogido por la pérdida de toda su agua celular. En el ejemplo mostrado, El 30 % del volumen celular es osmóticamente inactivo, compuesto por un 10 % de agua ligada (agua no osmótica) y un 20 % de sólidos celulares. Un estudio de ovocitos humanos usando un gráfico de Boyle-van't Hoff encontró que casi el 20% del agua celular es osmóticamente inactiva [REVISTA DE REPRODUCCIÓN Y FERTILIDAD; Newton,H; 117(1):27-33 (1999)].
Las células pueden tolerar la pérdida de agua osmóticamente activa, pero la eliminación del agua unida es extremadamente perjudicial para la viabilidad. Sin agua unida, las proteínas pierden su estructura y las membranas se fusionan [CRIOBIOLOGÍA; Sol,WQ; 38(4):372-385 (1999)]. Hay evidencia, sin embargo, de que la reducción del volumen celular por la pérdida de agua osmótica más allá de un nivel crítico causa daño que no puede atribuirse al daño electrolítico [CRIOBIOLOGÍA; Williams, AJ; 17(6):530-539 (1980)].
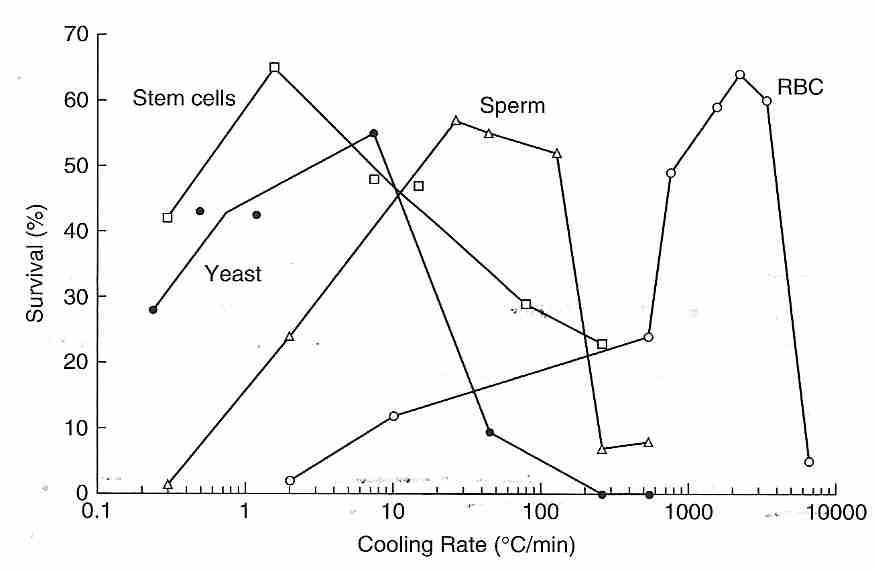 |
Los métodos de crioconservación clásicos (sin vitrificación) de la criobiología se dedican a congelar células o pequeñas colecciones de células (embriones) a una velocidad de enfriamiento que minimiza la pérdida de viabilidad. La ilustración indica que aproximadamente el 60 % de las células pueden sobrevivir con una velocidad de enfriamiento de 1 ºC/minuto (células madre), 25 ºC/minuto (esperma) o 5000 ºC/minuto (RBC, glóbulos rojos). El hielo se forma mucho más fácilmente (a temperaturas más altas) fuera de las células que dentro de las células porque los nucleadores son más fuertes y más abundantes fuera de las células. La concentración de sal isotónica en el cuerpo humano es de aproximadamente 0,9% de NaCl (cloruro de sodio), mientras que la temperatura de congelación eutécticade una solución de NaCl es 22% en peso. El hielo de agua pura se forma en el espacio extracelular de los tejidos, dejando una solución salina cada vez más concentrada, hasta que la concentración alcanza el 22 % en peso, momento en el que la mezcla eutéctica se congelará. La creciente concentración de sal extracelular en la porción no congelada hace que más agua abandone osmóticamente las células. Cuando la célula ha sido deshidratada de toda el agua osmóticamente activa, el agua unida restante y la proteína pueden vitrificar la célula.
La supervivencia celular generalmente cae a cero para velocidades de enfriamiento que son demasiado rápidas o demasiado lentas, dando una "curva de U invertida". Las velocidades de enfriamiento excesivamente rápidas pueden matar las células por daño osmótico a las membranas causado por la presión y la fricción de las moléculas de agua que salen. O el enfriamiento excesivamente rápido permite la formación de hielo dentro de las células, que es mucho más dañino que el hielo extracelular. Existe evidencia de que el daño de la membrana plasmática debido a una presión osmótica excesiva crea agujeros en la membrana que permiten que se forme hielo intracelularmente [ BIOPHYSICAL JOURNAL; MuldrewK; 66 (2 Pt 1): 532-541 (1994) ]. Sin embargo, con el enfriamiento ultrarrápido, el agua no tiene tiempo de salir de las células, y el enfriamiento ultrarrápido puede causar vitrificación intracelular; ambos efectos aumentan la viabilidad celular.CRIOBIOLOGIA; Dumont,F; 46(1):33-42 (2003) ]. Sin embargo, si el enfriamiento es demasiado lento, las células morirán por exposición prolongada a las concentraciones tóxicas de electrolitos que se forman fuera de la célula o por aplastamiento mecánico del hielo extracelular. El método de dos pasos de Farrant es enfriar rápidamente a una temperatura ligeramente bajo cero, mantener esa temperatura hasta que se establezca el equilibrio osmótico y luego reanudar el enfriamiento rápido.
La tasa de enfriamiento óptima es una función de la permeabilidad de la membrana al agua y la dependencia de la temperatura (energía de activación) de la permeabilidad de la membrana [ REPRODUCCIÓN HUMANA; Devireddy,R; 15(5):1125-1135 (2000) ]. La razón por la cual los glóbulos rojos (RBC) tienen una tasa de enfriamiento óptima tan alta para la supervivencia celular es porque tienen una gran cantidad de proteínas de canal de agua ( acuaporinas ) que permiten el paso rápido de agua a través de la membrana celular [ JOURNAL OF BIOLOGICAL CHEMISTRY; YangB; 276(1):624-628 (2001) ]. Las células madre, como la mayoría de las células, no tienen acuaporinas, por lo que el agua que cruza la membrana celular solo puede hacerlo por difusión a través de la bicapa de fosfolípidos .
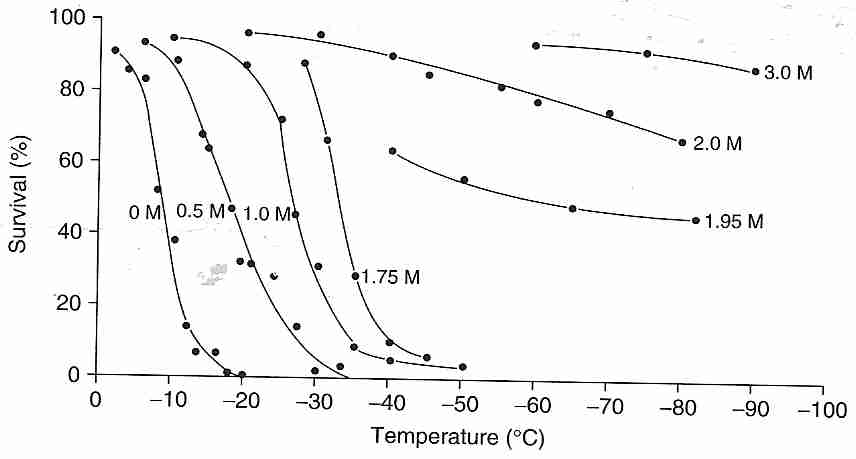 |
Los criobiólogos suelen utilizar crioprotectores para mejorar el proceso de crioconservación por congelación en lugar de vitrificación. Los criobiólogos buscan reducir (pero no eliminar) la formación de hielo mientras minimizan la exposición a la toxicidad de los crioprotectores . Como se muestra en la ilustración, el glicerol agregado a los glóbulos rojos humanos mueve la curva de supervivencia celular a temperaturas más bajas, e incluso elimina la destrucción de todas las células para concentraciones de 1,95 molar ( moles por litro) y mayores para enfriamiento lento (1,7 ºC/minuto) y descongelación rápida. La mera presencia de hielo en una solución puede provocar la desnaturalización de la proteína que se absorbe en el hielo, un fenómeno que se puede prevenir con pequeñas cantidades de crioprotector [ BIOPHYSICAL JOURNAL; Strambini, GB; 70(2):971-976 (1996)]
Aunque los crioprotectores están presentes en concentraciones insuficientes para vitrificar y proteger las células que se enfrían lentamente, no ofrecen protección a las células enfriadas a velocidades de enfriamiento excesivamente altas porque el agua no tiene tiempo suficiente para difundirse fuera de la célula y/o está dañando las membranas celulares por la velocidad de enfriamiento. la difusión osmótica. Los crioprotectores no solo se difunden a través de las membranas celulares a diferentes velocidades, sino que también afectan la velocidad con la que el agua atraviesa las membranas. Para el esperma humano, el agua atraviesa las membranas celulares unas tres veces más rápido con glicerol que con DMSO, y unas tres veces más rápido con etilenglicol que con glicerol a 22ºC [ BIOLOGÍA DE LA REPRODUCCIÓN; Gilmore,JA; 53(5):985-995 (1995) ]. Tanto el agua como los crioprotectores atraviesan las membranas celulares más lentamente a temperaturas más bajas.
Posiblemente, el crioprotector y la concentración crioprotectora más común utilizada por los criobiólogos es DMSO al 10 %. Los protocolos que usan DMSO al 10 % se han adaptado de la médula ósea a las células madre de la sangre del cordón umbilical [CRIOBIOLOGÍA; Caza;CJ; 46(1):61-75 y 76-87 (2003)]. Un protocolo común es enfriar a la tasa de enfriamiento óptima para DMSO al 10 % entre 0 °C y una temperatura de inmersión entre -30 °C y -40 °C, y luego sumergir la muestra en nitrógeno líquido a la temperatura de inmersión. Con la formación de hielo extracelular y la difusión de DMSO en las células deshidratadas, la concentración de DMSO en las células a la temperatura de inmersión podría ser de alrededor del 40 %.
A pesar de que ha habido cierto éxito en la vitrificación de órganos animales, muchos criobiólogos todavía luchan por crioconservar células individuales. Los huevos de pescado (ovocitos) son particularmente desafiantes debido a su alto contenido de lípidos y su gran tamaño. Un tamaño grande dificulta la aplicación de crioprotectores debido a la baja superficie disponible para la difusión en relación con el volumen celular. Para una esfera, el área superficial S = 4πr 2 y el volumen V = (4/3)πr 3 , lo que significa que S / V varía inversamente con r (radio). En otras palabras, a medida que aumenta el radio, disminuye la cantidad de área superficial en relación con el volumen.
Los embriones de pez cebra también son candidatos favoritos para la criopreservación mediante métodos de congelación. El pez cebra se ha convertido en un organismo modelo para estudiar el desarrollo y la genética de los vertebrados. Pero los embriones tienen una baja permeabilidad al agua y a los crioprotectores, y los embriones nunca se han crioconservado con éxito. Los métodos de criopreservación por congelación se han aplicado con éxito a otros embriones marinos como las ostras y los erizos de mar.
(Para ver un libro que resume la criobiología de vanguardia a partir de 2004, consulte LA VIDA EN ESTADO CONGELADO ).
tercero ENFRIAMIENTO A LA TEMPERATURA DE TRANSICIÓN DEL CRISTAL
![[Cambios de volumen específicos en T<SUB>m</SUB> y T<SUB>g</SUB>]](https://benbest.com/cryonics/glassy.gif) |
Mediante el uso de altas concentraciones de crioprotectores en células biológicas, tejidos y órganos, la solidificación al enfriarse a temperatura criogénica puede ser por vitrificación a un sólido vítreo en lugar de por congelación, y no habrá formación de cristales de hielo. El cambio de un líquido almibarado a un sólido vítreo que se produce a la temperatura de transición vítrea ( Tg ) se puede cuantificar en términos de un aumento repentino de la viscosidad. La viscosidad a Tg es de aproximadamente 10 12 Pascal-segundo o (equivalentemente) 10 13 Poise, ya que diez Poise equivalen a un Pascal-segundo. [ El peso como unidad de viscosidad es una reliquia del obsoleto sistema cgs , igual a (dina/cm 2) X segundo, pero todavía se usa mucho.] La T g es menos precisa que la temperatura del punto de fusión (T m ) en la medida en que un aumento de un orden de magnitud en la tasa de enfriamiento puede aumentar la T g en 3−5ºC. Las velocidades de enfriamiento más lentas dan tiempo a las moléculas para minimizar el "volumen libre". Los líquidos clasificados como "fuertes formadores de vidrio" como la sílice (SiO 2 ) muestran solo un pequeño cambio en la viscosidad a T g , mientras que los llamados líquidos "frágiles" como los polímeros muestran cambios muy grandes en la viscosidad a T g [NATURE 410: 259-267 (8 de marzo de 2001)].
Otras dos variables que muestran cambios distintivos en Tg son el volumen específico y la capacidad calorífica específica. Volumen específico significa volumen por unidad de masa, es decir, m 3 /kg en unidades SI (y MKS). La palabra específico significa "por unidad de masa", a diferencia de "por mol". La mayoría de los materiales experimentan una disminución del volumen específico con la disminución de la temperatura. A Tm hay una fuerte caída en el volumen específico seguida de una clara disminución en la tasa de disminución del volumen específico con la disminución de la temperatura. Por el contrario, la región sobre la que se produce T g muestra sóloun cambio en la tasa de disminución del volumen específico con la disminución de la temperatura.
A T g también hay una clara disminución en la tasa de disminución de la capacidad calorífica específica con la disminución de la temperatura. La capacidad calorífica específica se refiere a la cantidad de calor agregado o eliminado por unidad de masa para producir un cambio unitario de temperatura, en contraste con la capacidad calorífica molar, que es la cantidad de calor por mol de material para producir un cambio unitario de temperatura. (El término capacidad calorífica específica generalmente se usa en las formas abreviadas "calor específico" o "capacidad calorífica". Energía específica capacidad sería un término más preciso porque la temperatura del gas se puede cambiar por trabajo de compresión, no solo por calor). El agua líquida tiene una capacidad calorífica específica muy alta en comparación con la mayoría de los otros materiales. A 4,2 kilojulios por kilogramo-kelvin, el agua tiene más de diez veces la capacidad calorífica específica del cobre. (La cantidad de calor necesaria para calentar agua 1ºC a 14,5ºC era la definición original de caloría , pero una caloría ahora se define como 4,184 julios). (El glicerol tiene aproximadamente la mitad de la capacidad calorífica específica y la mitad de la conductividad térmica del agua).
La alta capacidad de calor específico de los océanos de la tierra evita grandes cambios de temperatura en nuestro planeta. El gran contenido de agua del tejido animal también protege contra los cambios rápidos de temperatura en ambientes cálidos o fríos. La capacidad calorífica específica de la porción sólida (sin agua) de la carne fresca es de 0,84 y, combinada con la porción de agua, le da a la carne fresca una capacidad calorífica específica de 3,14, que podría tomarse como un indicador de la capacidad calorífica específica de un paciente de criónica. La capacidad calorífica específica del glicerol (y crioprotectores similares) es de aproximadamente 2,4. Un estudio de las capacidades caloríficas específicas y la disminución de las capacidades caloríficas específicas de los crioprotectores y los pacientes criónicos podría ser útil para diseñar equipos científicos de refrigeración para su uso en criónica.
La capacidad de calor específico de todos los materiales disminuye a un valor de cero a una temperatura de cero Kelvin, lo que significa que una pequeña cantidad de calor podría causar un gran aumento de temperatura en cualquier material cercano al cero absoluto. El cambio en la tasa de cambio de la capacidad calorífica específica es tan distintivo en Tg que los científicos que estudian los crioprotectores lo utilizan para determinar Tg . El instrumento que mide esta "firma térmica" se llama Calorímetro de Barrido Diferencial ( DSC ). Para la mayoría de las sustancias, el cambio en la tasa de cambio de la capacidad calorífica específica en T g aumenta con el peso molecular y T g aumenta a medida que aumenta el peso molecular [PHARMACEUTICAL RESEARCH 11(1):54-59 (1994)].
[Para una discusión más detallada de T g , consulte mi ensayo Vitrification in Cryonics and Fragility thy name is glass ]
IV. TASA DE ENFRIAMIENTO CRÍTICO PARA VITRIFICACIÓN
Las temperaturas criogénicas pueden preservar los tejidos de los mamíferos esencialmente inalterados durante muchos siglos, si no muchos milenios [AMERICAN JOURNAL OF FISIOLOGY; Mazur,P; 247 (3 Pt 1): C125-C142 (1984)]. Aunque la vitrificación por encima de las temperaturas criogénicas da como resultado un estado sólido, aún pueden ocurrir reacciones químicas de deterioro en el tejido vitrificado a temperaturas más altas [INVESTIGACIÓN FARMACÉUTICA; Streefland,L; 15(6):843-849 (1998)].
¿Con qué rapidez debe enfriarse un paciente de criónica en el descenso de 10 ºC a −196 ºC? Para responder científicamente a esta pregunta, es útil estudiar las propiedades de los materiales en cuestión, a saber, el agua, el crioprotector y el tejido biológico. El agua sin purificar, por supuesto, tiene una temperatura de congelación cercana a los 0ºC, pero la congelación es lo que los crionicistas intentan evitar o minimizar. En cambio, los crionicistas están tratando de vitrificar tanto como sea posible, es decir, producir una solidificación vítrea en lugar de cristalina para evitar daños mecánicos por los cristales de hielo. El agua se puede vitrificar enfriándola a una velocidad de alrededor de 3 millones de ºC por segundo [JOURNAL OF MICROSCOPY 143(Pt 1):89-102 (1986)] hasta aproximadamente -138ºC, pero esta velocidad de enfriamiento no es práctica para la criónica. Afortunadamente, la tasa de enfriamiento requerida para producir un sólido vitrificado (vítreo) en lugar de un sólido cristalino es mucho menor para las soluciones que contienen crioprotector que para el agua pura. La tasa de enfriamiento más lenta que produce vitrificación (previene la formación de hielo) se conoce comovelocidad crítica de enfriamiento . (Para obtener más detalles sobre el proceso de vitrificación, consulte mis ensayos Vitrification in Cryonics y Lessons for Cryonics from Metallurgy and Ceramics ).
Al igual que el agua pura, el crioprotector glicerol tiene una temperatura de congelación cercana a los 0ºC, pero las mezclas de glicerol y agua se congelan a temperaturas más bajas. Una solución de glicerol al 50 % p/p (peso/peso) tiene una temperatura de congelación/fusión (T m ) de −23 ºC. La mezcla con la temperatura de congelación más baja tiene aproximadamente un 66 % de glicerol y se congela a unos −46 ºC. Pero muchos crionicistas esperan algo mucho mejor que las mezclas congeladas de glicerol y agua. Lo que es más interesante es la temperatura de transición vítrea ( Tg , la temperatura a la que la mezcla de crioprotector/agua se endurece de un líquido almibarado a un vidrio sólido). Para mezclas de glicerol T gestá cerca de -110ºC. La viscosidad cada vez más alta de las mezclas de agua/glicerol a temperaturas más bajas, y la ausencia de nucleación , significa que las mezclas se pueden sobreenfriar por debajo de la temperatura de congelación/fusión sin congelarse. (T g es típicamente alrededor de dos tercios del valor de T m en una escala de temperatura Kelvin para sustancias que vitrifican). vitrificará a T g en lugar de congelarse a una temperatura más alta.
|
Una solución de glicerol al 50% tiene una velocidad crítica de enfriamiento de 100ºC por minuto. Al agregar un 6 % p/p de polietilenglicol [PEG400] de bajo peso molecular (400 gramos/mol), se puede lograr una velocidad de enfriamiento crítica de 50 °C/min para una solución de glicerol al 44 %. El butano-2,3-diol (2,3-BD), sin embargo, es un crioprotector mucho más vitrificable que el glicerol. Una solución que contiene solo 28,8 % de 2,3-BD tiene una velocidad crítica de enfriamiento de 270 ºC/min y la adición de PEG400 reduce la velocidad a 20 ºC/min [ CRYOBIOLOGY 29(5):585-598 (1992) ]. Sin embargo, el 2,3-BD es bastante tóxico y, por este motivo, los investigadores de 21st Century Medicine (21CM) han preferido utilizar altas concentraciones de crioprotectores con menor capacidad de formación de vidrio. Sin embargo, incluso velocidades de enfriamiento de 20ºC/min han estado mucho más allá del alcance de la práctica de la criónica.
Las soluciones de vitrificación más potentes, como M22 y CI−VM−1, han permitido a los crionicistas lograr la vitrificación a velocidades de enfriamiento alcanzables. De manera similar, los criobiólogos han logrado la vitrificación de embriones y ovocitos al reducir la concentración de crioprotector vitrificante (reduciendo así la toxicidad) y acelerar la velocidad de enfriamiento. Los volúmenes más pequeños de muestras en crioprotector se pueden enfriar a velocidades de enfriamiento más rápidas que los volúmenes más grandes [ ENDOCRINOLOGÍA MOLECULAR Y CELULAR; Arav,A; 187(1-2):77-81 (2002) ].
Cuando se usaba glicerol en criónica, era deseable enfriarlo lo más rápido posible hasta la temperatura de congelación de la concentración estimada de glicerol (no inferior a -46ºC). Debido a que es deseable que la congelación ocurra en el espacio extracelular en lugar de intracelularmente (lo que es mucho más dañino), el enfriamiento por debajo de la temperatura de congelación estimada para las concentraciones de glicerol utilizadas en criónica no debería haber sido más rápido que 1,0 °C/minuto para dar tiempo a la congelación. difusión desde las células que acompaña a la congelación extracelular. El enfriamiento a velocidades más lentas es una compensación entre la toxicidad del crioprotector y el riesgo de cristalización.
Aunque nunca se ha aplicado en criónica o criobiología, un campo eléctrico oscilante puede reducir la formación de hielo durante el enfriamiento rápido. Se ha utilizado un campo eléctrico oscilante para reducir la cantidad de hielo que se forma al sumergir muestras de 1,5 microlitros de etilenglicol (EG) en nitrógeno líquido. La formación de hielo se redujo aproximadamente un 56 % para una solución de EG de 3,5 molar y se redujo aproximadamente un 66 % para una solución de EG de 4,5 molar [ CRIOBIOLOGÍA; Jackson,JH; 34(4):363-372 (1997) ].
Sin embargo, al vitrificar crioprotectores en pacientes con criónica (que siempre tienen agentes nucleantes en sus cuerpos), el enfriamiento debe ser lo más rápido posible a la temperatura de transición vítrea ( Tg ) para evitar la formación de hielo. La velocidad de enfriamiento no necesitaría ser tan rápida para una solución de vitrificación pura, pero la perfusión no puede ser perfecta para los pacientes con criónica y, sin duda, habrá concentraciones más bajas de crioprotector vitrificante en muchos tejidos. Sin embargo, el aumento exponencial de la toxicidad de los crioprotectores cuando se enfría a Tg reduce en gran medida el peligro de cristalización cerca de Tg [ ANNALS OF BIOMEDICAL ENGINEERING; Rabin,Y; 33(9):1213-1228 (2005)].
Justo por debajo de la temperatura de transición vítrea, el enfriamiento debe nivelarse rápidamente para evitar el agrietamiento por estrés térmico. Permanecer justo por debajo de la T g durante un tiempo puede permitir que se alivie la tensión térmica (recocido) antes del enfriamiento posterior. Y el enfriamiento posterior debe ser lo suficientemente lento como para no causar grietas por tensión térmica. En teoría, el agrietamiento podría evitarse mediante un enfriamiento lo suficientemente lento, pero debido a que los enlaces de hidrógeno se rompen fácilmente, una velocidad de enfriamiento para evitar el agrietamiento podría llevar meses, lo cual no es práctico. Entonces, los pacientes de criónica se enfrían a la temperatura del nitrógeno líquido durante un período de aproximadamente una semana. El Instituto Cryonics tiene cajas de enfriamiento controladas por computadoraque permiten la preprogramación de la secuencia de pasos de enfriamiento deseada en un protocolo de enfriamiento.
Se ha demostrado que la solución de vitrificación M22 de 21st Century Medicine [CRYOBIOLOGY 48:157-178 (2004)] tolera el superenfriamiento sin riesgo de formación de hielo para un volumen de 2 litros de crioprotector puro con una velocidad de enfriamiento de 0,15 ºC por minuto durante 18 horas . Solo a velocidades de enfriamiento de 0,10ºC por minuto se hizo visible una pequeña cantidad de cristales de hielo. La tasa crítica de calentamiento de 0,4 ºC por minuto para evitar la desvitrificación fue suficiente para un volumen de 10 ml de M22. (Para obtener detalles sobre el problema de desvitrificación asociado con la tasa crítica de calentamiento, consulte El problema de la desvitrificación ).
V. MÉTODOS DE ENFRIAMIENTO EN CRIONICA
Solo hay dos modos de transferencia de calor mediante los cuales los objetos pueden calentarse o enfriarse: conducción y radiación. La conducción es la transferencia de energía térmica desde (o hacia) moléculas más energéticas hacia (o desde) moléculas adyacentes menos energéticas mediante interacción cinética (la temperatura es una medida de la energía cinética molecular). La radiación es la transferencia de energía por medio de ondas electromagnéticas (fotones). La radiación de microondas es una forma superior de transferencia de energía térmica en el sentido de que puede penetrar profundamente debajo de la superficie. El enfriamiento por microondas eleva las temperaturas uniformemente en lugar de hacerlo a través de la conducción desde la superficie. Durante mucho tiempo soñé con una forma inversa de microondas que pudiera enfriar a los pacientes de criónica de manera uniforme en lugar de hacerlo a través de la conducción en la superficie.
En criónica, enfriamos a los pacientes con convección , una combinación de conducción y movimiento de fluidos. En la convección, un objeto sólido (como un paciente de criónica) se enfría con un fluido (líquido o gas) que circula rápidamente, de modo que el fluido puede alejar el calor de la capa de conducción que rodea al objeto sólido. Una persona que enfrenta un viento frío se enfriará más rápidamente de frente que de espalda porque la convección del aire en movimiento se suma al efecto de conducción del contacto con la temperatura ambiente. En el enfriamiento de un paciente recién desanimado de la temperatura del cuerpo humano (37ºC) a 10ºC, el enfriamiento por circulación rápida de agua helada es mucho más efectivo que el enfriamiento por bolsas de hielo o por agua estancada debido al efecto de convección.
La fórmula que rige la convección es la Ley de enfriamiento de Newton, que iguala la tasa de transferencia de calor a h A ( T s − T f ) donde T s es la temperatura inicial (cabeza o cuerpo de un paciente criónico), T f es la temperatura final ( temperatura del medio de enfriamiento, por ejemplo, agua helada o gas nitrógeno frío), A es el área superficial del sólido y h es una variable que depende de la velocidad de movimiento del fluido, así como de la conductividad térmica y la capacidad calorífica de los materiales . Un movimiento fluido más rápido y una conductividad térmica más alta aumentarán el valor de h. En medicina forense, es una regla general que un cuerpo humano se enfría aproximadamente el doble de rápido en agua tranquila, y aproximadamente tres veces más rápido en agua corriente, que lo que se enfriaría en el aire. Esta guía no especifica la temperatura del agua ni el caudal, que para la criónica debe ser la temperatura del agua helada y un flujo tan rápido como sea práctico.
La conductividad térmica es una cuantificación de la capacidad de un material para conducir el calor. Los materiales que conducen fácilmente el calor (como los metales) se distinguen de los aislantes con baja conductividad térmica (como el poliestireno expandido, la espuma de poliestireno). El agua tiene una conductividad térmica baja en comparación con los metales, pero tiene una conductividad térmica alta en comparación con la mayoría de los disolventes orgánicos. La conductividad térmica del agua a 25ºC (0,61 Watts por metro-Kelvin) es más del doble que la del glicerol o la del etilenglicol (0,29 y 0,26 W/m−K, respectivamente) y es más de 20 veces mayor que la del gas nitrógeno (0,026 W/m−K). Entre 37ºC (temperatura corporal) y 0ºC la conductividad térmica del agua desciende más de un 10% (0,625 a 0,561 W/m−K).
La Ley de Enfriamiento de Newton predice que la velocidad de enfriamiento es mayor al comienzo del enfriamiento cuando T s es mucho mayor que T f , y la velocidad de enfriamiento disminuye exponencialmente a partir de entonces. Esto sería óptimo para fines de criónica. La tasa metabólica se reduce a la mitad por cada 10ºC de descenso de la temperatura, pero la reducción de la peroxidación lipídica por enfriamiento es mayor que la reducción de la tasa metabólica. Experimentos en jerbos indican que un descenso de la temperatura de 37ºC a 31ºC casi triplica el tiempo que las neuronas pueden tolerar la isquemia [MEDICINA DE TERAPIA INTENSIVA; Takeda,Y; 31(1):255-260 (2003)]. Las ratas sometidas a 2 horas de isquemia del tejido cerebral mostraron una reducción significativa del déficit neurológico como resultado de una reducción de la temperatura corporal de solo 4ºC durante 5 horas, que comenzó una hora después del inicio de la reperfusión [ STROKE; Kollmar,R; 33(7):1899-1904 (2002) ]. Los globos oculares de los cerdos muestran una curva de enfriamiento exponencial en las primeras 13 horas después de la muerte [ FISIOLOGÍA EXPERIMENTAL; Kaliszan,M; 90(5):727-738 (2005) ].
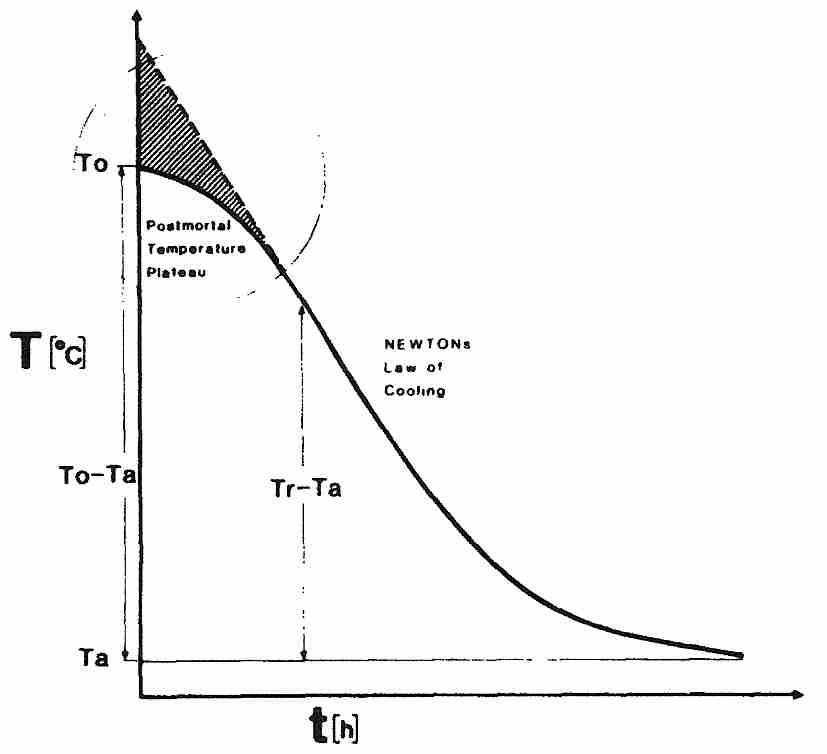 |
La Ley de Enfriamiento de Newton, sin embargo, no describe adecuadamente el enfriamiento de un paciente criónico, especialmente en la etapa inicial más crítica inmediatamente después de la muerte legal. Aunque el corazón ha dejado de latir, la mayoría de las células del cuerpo todavía están metabólicamente activas y generan calor. La piel y la grasa subcutánea se han diseñado para proporcionar un buen aislamiento. Aunque el cuerpo tiene un alto contenido de agua, el tejido corporal tiene una conductividad térmica más baja que el agua pura. Un cuerpo humano que inicialmente está a temperatura ambiente en el momento del paro cardíaco, y que no está sujeto a ningún otro medio de enfriamiento que no sea el aire a temperatura ambiente, tenderá a permanecer en una meseta de temperatura corporal normal durante un tiempo antes de entrar en una curva de enfriamiento exponencial hacia temperatura ambiente. Una persona acostada boca arriba expondrá el 80 % de su superficie al enfriamiento de la superficie, mientras que en la posición fetal solo se expone el 60 % de la superficie. Aunque el paciente de criónica se encuentra idealmente en un baño de hielo inmediatamente después de la muerte legal (y siendo apoyado metabólicamente por una máquina de circulación extracorpórea), debe oponerse a la inercia térmica debida al metabolismo generador de calor.
Debido a que el metabolismo celular (y la generación de calor celular) es más alto inmediatamente después de la muerte legal, la resistencia inicial al enfriamiento da como resultado una curva en forma de sigmoide, con la meseta inicial no newtoniana en transición gradual a la forma newtoniana [FORENSIC SCIENCE INTERNATIONAL; Henssge,C; 38(3-4):209-236 (1988) y [ FORENSIC SCIENCE INTERNATIONAL; Karhunen,PJ; 176(2-3):e17-e22 (2008) ]. Afortunadamente, la meseta en el cerebro es solo alrededor de un tercio de lo que se observa en el cuerpo en general [FORENSIC SCIENCE INTERNATIONAL; Al-Alousi, LM; 125(2-3):237-244 (2002)].
La Ley de enfriamiento de Newton es más directamente aplicable cuando se enfría un paciente criogénico después de la perfusión de vitrificación (normalmente desde alrededor de 0 ºC hasta la temperatura de transición vítrea, T g , que es de aproximadamente -125 ºC para vitrificar crioprotectores). Hay poca inercia térmica debido al metabolismo generador de calor a estas temperaturas. Pero intentar acelerar el enfriamiento bajando la temperatura ( Tf ) por debajo de Tg para una muestra vitrificable grande (paciente criogénico) aumenta la probabilidad de fracturas superficiales [ CRYOBIOLOGY 27(5):492-510 (1990) ].
Durante muchos años, Alcor enfrió a los pacientes criónicos con un aceite de silicona ( polidimetil siloxano , también conocido como dimeticona) que permanece líquido hasta unos −100ºC. Este material no tóxico es similar a la silicona que se usa en el calafateo del baño y como espesante en los champús (agregue ácido bórico [H 3 BO 3] y obtienes "masilla tonta"). Alcor usó un baño de aceite de silicona para enfriar a los pacientes a una velocidad que mantendría una diferencia de temperatura de 10 ºC entre una sonda de temperatura en el centro del cerebro del paciente y la temperatura de la superficie, una velocidad de enfriamiento de alrededor de 0,1 ºC/min. Esta tasa de enfriamiento puede haber aliviado algunas de las tensiones que surgen de la congelación de las mezclas de glicerol/agua. (Debido a que el aceite de silicona es tan costoso, Alcor lo reciclaría utilizando polvo de yeso de París, sulfato de calcio, para precipitar el agua y otros contaminantes). Con el uso de cócteles crioprotectores superiores y bloqueadores de hielo, se cree que una cantidad insignificante de hielo se forma en los pacientes neuro de Alcor, por lo que el problema del daño por agrietamiento relacionado con el estrés por encima de T gha sido eliminado por neuros. Más importante aún, el enfriamiento se puede hacer más rápido con la vitrificación porque ya no es necesario esperar a que la ósmosis iguale las concentraciones de crioprotector intra/extracelular de la congelación.
Ahora Alcor y el Instituto Cryonics hacen enfriamiento por convección que enfría la cabeza a una temperatura cercana a Tg a una velocidad de más de 0,4ºC/min usando vapor de nitrógeno líquido. Una alta tasa de flujo de gas puede compensar la baja conductividad térmica y la capacidad calorífica del gas nitrógeno líquido. Siempre que la temperatura del vapor no esté por debajo de T g , no debe haber solidificación en la superficie del paciente de criónica que podría provocar tensiones y grietas. (Para obtener detalles sobre las cajas de enfriamiento utilizadas por el Instituto Cryonics, consulte Cajas de enfriamiento controladas por computadora en CI ).
Aunque 21CM ha descubierto mezclas crioprotectoras que permiten la vitrificación con velocidades de enfriamiento de menos de 1 ºC/min, ningún método de enfriamiento externo puede enfriar el interior de un paciente de criónica de cuerpo entero a una velocidad mucho más rápida que aproximadamente 0,2 ºC/min, que impide la vitrificación de pacientes de cuerpo entero utilizando mezclas crioprotectoras existentes y refrigeración externa. Ningún método de enfriamiento externo puede enfriar el interior de un paciente con criónica solo de cabeza mucho más rápido que 1ºC/min, pero esta velocidad es lo suficientemente rápida como para permitir la vitrificación.
Se podrían lograr velocidades de enfriamiento más rápidas mediante el uso de perfluorocarbono, una sustancia con una viscosidad extremadamente baja y que permanece en estado líquido hasta al menos -100ºC. En lugar de depender de la conductividad térmica lenta de la superficie del paciente de criónica, los perfluorocarbonos a baja temperatura pueden perfundirse a través de los vasos sanguíneos. Mike Darwin hizo experimentos con animalescon este procedimiento se lograron velocidades de enfriamiento de todo el cuerpo calculadas en 9ºC/min a 0ºC, cayendo a 1ºC/min a −90ºC. Para los cerebros calculó sus tasas en 50ºC/min a 0ºC cayendo a 5ºC/min a −90ºC. Sin embargo, el enfriamiento puede ser menos que completamente uniforme, porque una vez que el perfluorocarbono desplaza el líquido crioprotector de algunos vasos, puede circular libremente mientras deja otros vasos aún obstruidos con crioprotector. Como se sugiere en la Patente 6.274.303 (que patenta el uso de refrigeración con perfluorocarbono para órganos y tejidos grandes), el uso de una serie de perfluorocarbonos de viscosidad decreciente es un medio para prevenir este problema. La misma patente afirma que el enfriamiento de perfluorocarbono vascular puede enfriar diez veces más rápido que el enfriamiento externo.
![[GRÁFICO DE COMPARACIÓN DE MÉTODOS DE ENFRIAMIENTO]](https://benbest.com/cryonics/external.gif) |
El enfriamiento inicial de los pacientes de criónica desde la temperatura del cuerpo humano en el momento de la muerte legal hasta alrededor es extremadamente crítico para reducir la cantidad de daño isquémico . Embalar a un paciente de criónica en hielo dará como resultado una velocidad de enfriamiento que no supere los 0,064 ºC/minuto, lo que llevaría de 6 a 8 horas para enfriar a 20 ºC. El uso de un batidor y un baño de hielo puede enfriar a 15 °C, y la adición de un calamar puede enfriar potencialmente a 10 °C en poco más de 2 horas (el paciente A-1049 pesaba 2/3 del peso de los otros dos pacientes, lo que resultaría en enfriamiento más rápido). El uso de un bypass cardiopulmonar para enfriar internamente a un paciente criónico con una solución de lavado de sangre fría puede reducir el tiempo de enfriamiento a una hora, pero se requiere media hora de cirugía, y se produce mucho daño isquémico durante la media hora de cirugía. En 2011Suspended Animation, Inc. anunció que estaba lista para implementar un sistema de enfriamiento de lavado pulmonar que había sido desarrollado para su uso por Critical Care Research, una compañía de California financiada por Life Extension Foundation . Los pulmones tienen un área de superficie del tamaño de una cancha de tenis que es eficiente tanto para el intercambio de calor como para el intercambio de gases. El perfluorocarbono frío recirculado a través de los pulmones puede enfriar a un paciente criónico a 1,2 ºC/minuto. El lavado pulmonar con perfluorocarbono combinado con un baño de hielo y un golpecito puede enfriar a un paciente criónico a 5 °C en 30 a 45 minutos sin el retraso de la cirugía asociado con el enfriamiento del bypass cardiopulmonar.
Algo parecido a un efecto similar a un microondas inverso podría ser posible mediante el uso de la desmagnetización adiabática . Un paciente de criónica podría perfundirse con una solución compuesta no solo de crioprotector sino también de una sal paramagnética como el alumbre de amonio férrico en un campo magnético. Al disminuir gradualmente la fuerza del campo magnético, los iones de sal se desordenan, atrayendo uniformemente el calor por todo el cuerpo del paciente criónico, no solo desde la superficie. Este u otros mecanismos novedosos de enfriamiento podrían ser potencialmente de gran beneficio para resolver el problema del enfriamiento rápido de grandes objetos biológicos.
Es posible que el daño estructural pueda mantenerse a un mínimo tolerable incluso sin una vitrificación completa. El esperma de toro se crioconserva comercialmente enfriándolo a 15 ºC/min (mucho menos que la tasa crítica de enfriamiento) de 5 ºC a -100 ºC, seguido de inmersión en nitrógeno líquido. Las membranas se protegen con los disacáridos sacarosa y trehalosa [ CRYOBIOLOGY 37(3):219-230 (1998) ]. No es necesario que todos los espermatozoides sobrevivan para que el procedimiento sea práctico cuando se utilizan grandes cantidades de espermatozoides. En aplicaciones criobiológicas en las que se tolera algo de congelación, se observa una curva de supervivencia en forma de U invertida: las células enfriadas demasiado lentamente o demasiado rápido sufren daños [FERTILITY AND STERILITY 60(5):911-918 (1993)].
La congelación demasiado rápida no permite suficiente tiempo para que el agua se difunda desde las células y se congele extracelularmente, y es la congelación intracelular la que causa el mayor daño. Sin embargo, con una congelación más rápida, los cristales de hielo que se forman son más pequeños y menos dañinos. Los cristales grandes en los alimentos que se congelan demasiado lentamente dañan las paredes celulares, lo que provoca la degradación de la textura y la pérdida de jugos naturales.
Durante años, muchos crionicistas creyeron que el glicerol 3,72 molar (27,2 % v/v) es óptimo porque permitiría un 60 % de agua congelada en el espacio extracelular mientras que el agua intracelular se vitrificaba. La microscopía óptica pareció confirmar esta teoría, pero la microscopía electrónica la refutó más tarde. A partir de entonces, algunas organizaciones de criónica encontraron mejores resultados al usar la concentración más alta posible de glicerol (poco más de 7 molar). (Anteriormente, algunos crionicistas habían sostenido la creencia errónea de que las concentraciones de glicerol demasiado altas disuelven las membranas celulares). para lograr concentraciones muy por encima del 55 % v/v (7,5 molar) en un paciente de criónica. Entonces, cuando se usa glicerol como crioprotector, el enfriamiento debe realizarse a aproximadamente 0. 5ºC por minuto a la temperatura de solidificación y luego a razón de 0,1ºC a 0,2ºC por minuto a temperaturas más bajas. Cuanto más rápido se pueda alcanzar la temperatura de solidificación, menos tiempo habrá para la toxicidad del crioprotector y el daño isquémico (entre otras reacciones indeseables), y mayor será la posibilidad de sobreenfriamiento a una temperatura de solidificación más baja. Pero si la velocidad de enfriamiento es superior a 0,5 ºC por minuto, es posible que no haya tiempo suficiente para que las células se deshidraten, lo que resultará en una congelación intracelular dañina en lugar de una congelación en el espacio extracelular. Cuanto más rápido se pueda alcanzar la temperatura de solidificación, menos tiempo habrá para la toxicidad del crioprotector y el daño isquémico (entre otras reacciones indeseables), y mayor será la posibilidad de sobreenfriamiento a una temperatura de solidificación más baja. Pero si la velocidad de enfriamiento es superior a 0,5 ºC por minuto, es posible que no haya tiempo suficiente para que las células se deshidraten, lo que resultará en una congelación intracelular dañina en lugar de una congelación en el espacio extracelular. Cuanto más rápido se pueda alcanzar la temperatura de solidificación, menos tiempo habrá para la toxicidad del crioprotector y el daño isquémico (entre otras reacciones indeseables), y mayor será la posibilidad de sobreenfriamiento a una temperatura de solidificación más baja. Pero si la velocidad de enfriamiento es superior a 0,5 ºC por minuto, es posible que no haya tiempo suficiente para que las células se deshidraten, lo que resultará en una congelación intracelular dañina en lugar de una congelación en el espacio extracelular.
El envío de pacientes criónicos en nitrógeno líquido no es factible, pero las soluciones de vitrificación utilizadas para criónica suelen ser lo suficientemente estables como para que los pacientes criónicos vitrificados puedan enviarse a temperatura de hielo seco. El hielo seco es aproximadamente 1,5 veces más denso que el hielo de agua a la temperatura de sublimación del hielo seco, pero la capacidad calorífica específica del hielo de agua es aproximadamente el doble que la del hielo seco. Esta consideración podría sugerir que sería mejor enfriar el hielo de agua a la temperatura del hielo seco para el envío. Pero esto ignora el efecto de enfriamiento del calor latente de sublimación del hielo seco. Por lo tanto, se prefiere el envío en hielo seco. Los contenedores de envío deben permitir cierta ventilación del dióxido de carbono sublimado.
VI. ESTRÉS Y TENSIÓN A BAJA TEMPERATURA
 |
Para los pacientes vitrificados por debajo de Tg y para los pacientes no vitrificados cargados con mezclas crioprotectoras que se han congelado a temperaturas más altas, los problemas de estrés que conducen al agrietamiento pueden convertirse en una preocupación importante. En mecánica de materiales, el estrés cuantifica la fuerza por unidad de área en un sólido, al igual que la presión cuantifica la fuerza por unidad de área en un gas o líquido. El estrés usa las mismas unidades que la presión : fuerza por unidad de área (newtons por metro cuadrado en unidades SI, llamadas Pascales ). La deformación es una medida del alargamiento de un material sólido bajo tensión. (Estar de pie en un trampolín crea estrés. La flexión del trampolín es la tensión .)
La rigidez del material ( módulo de Young , llamado módulo de elasticidad , pero mejor descrito como módulo de inelasticidad ) se cuantifica como la relación entre la tensión y la deformación. La tensión puede resultar no solo del estrés por presión, sino también del estrés por expansión térmica. El coeficiente de expansión térmica es una propiedad de los materiales, y para el hielo es muy alto. El coeficiente de expansión térmica del hielo es más de cinco veces mayor que el del vidrio sodocálcico de la cristalería estándar, lo que significa que el hielo puede provocar graves tensiones. El estrés por expansión térmica es la razón principal por la que la cristalería ordinaria se rompe tan fácilmente cuando se calienta. Reemplazando parte de la soda (Na 2O) y cal (CaO) de vidrio de cal sodada con óxido de boro (B 2 O 3 ) da como resultado pyrex , un vidrio con un tercio de la expansión térmica de la cal sodada y mucho más resistente al choque térmico. (El vidrio de cal sodada tiene aproximadamente la misma capacidad calorífica específica que el pirex y un 20 % más de conductividad térmica, por lo que claramente es la diferencia de expansión térmica la que más contribuye a la resistencia al choque térmico).
|
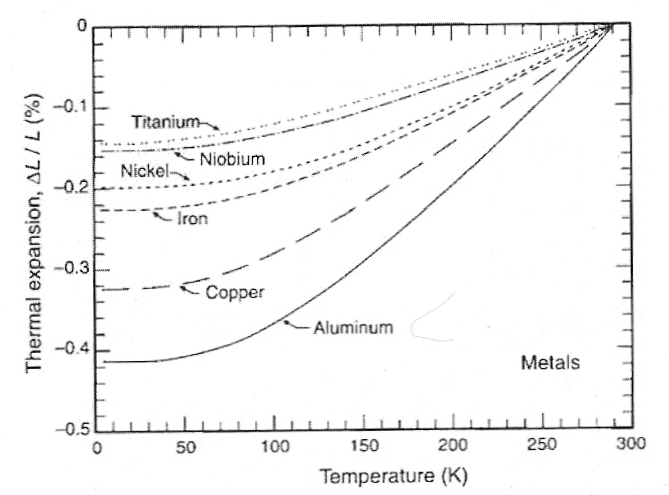
A medida que baja la temperatura, los materiales generalmente muestran una expansión térmica negativa ( es decir , una contracción térmica) en volumen, que se puede cuantificar a lo largo de una dimensión (contracción térmica lineal). Por ejemplo, en comparación con su longitud a la temperatura del agua helada (293 K = 0 ºC), el aluminio se contraerá un 0,2 % a 200 K (−73 ºC) y un 0,4 % a 80 K (−193 ºC, cerca de la temperatura de ebullición del nitrógeno líquido). Por el contrario, el pirex muestra una contracción mucho menor: alrededor del 0,027 % a 200 K (−73 ºC) y del 0,054 % a 80 K (−193 ºC). Teflón (que forma enlaces de hidrógeno muy fuertes), por el contrario, muestra una contracción térmica considerablemente mayor: 1,24% a 200 K (−73ºC) y 1,93% a 80 K (−193ºC). El enlace de hidrógeno (y la contracción térmica) del nailon es probablemente más comparable a lo que se esperaría de los tejidos biológicos y los crioprotectores. (Datos del Capítulo 2 de CRIOGENIA DE HELIO .)
La conductividad térmica a la temperatura del nitrógeno líquido es casi cuatro órdenes de magnitud mayor para el cobre en comparación con los materiales no metálicos y no cristalinos como el nailon, el teflón, el tejido biológico o los crioprotectores. Los metales tienen una alta conductividad térmica debido a los electrones, mientras que la conductividad térmica del cristal se debe a los fonones . El diamante sintético puro tiene una conductividad térmica casi cinco veces mayor que la plata.(a pesar de la muy baja conductividad eléctrica del diamante) debido a los fonones de la red. El agua tiene una conductividad térmica que es casi una milésima parte de la de la plata, pero el agua tiene aproximadamente el doble de la conductividad térmica del glicerol y aproximadamente cuatro veces la conductividad térmica del caucho. Las sustancias con baja conductividad térmica son aislantes térmicos. Las sustancias con baja conductividad térmica (como las sustancias con alta expansión térmica) desarrollan más estrés térmico durante el enfriamiento en comparación con las sustancias con mayor conductividad térmica.
La resistencia del material al agrietamiento también es función de la ductilidad o fragilidad del material. El hielo y los vasos se encuentran entre los materiales más frágiles, menos dúctiles. Los materiales dúctiles pueden soportar mucha más deformación plástica antes de la fractura que los materiales frágiles. Casi todos los materiales se vuelven menos dúctiles, cada vez más frágiles, con la disminución de la temperatura.
Con baja conductividad térmica y enfriamiento por convección en la superficie del paciente de criónica, las diferencias en la conducción térmica entre la superficie y el interior pueden provocar estrés térmico y, en última instancia, agrietamiento, si las velocidades de enfriamiento son demasiado rápidas. Los vidrios tienen una conductividad térmica más baja que los materiales cristalinos, lo que hace que el problema sea más grave para los pacientes con criónica completamente vitrificados que para los pacientes con criónica parcialmente congelados, a pesar de la menor expansión térmica de los vidrios.
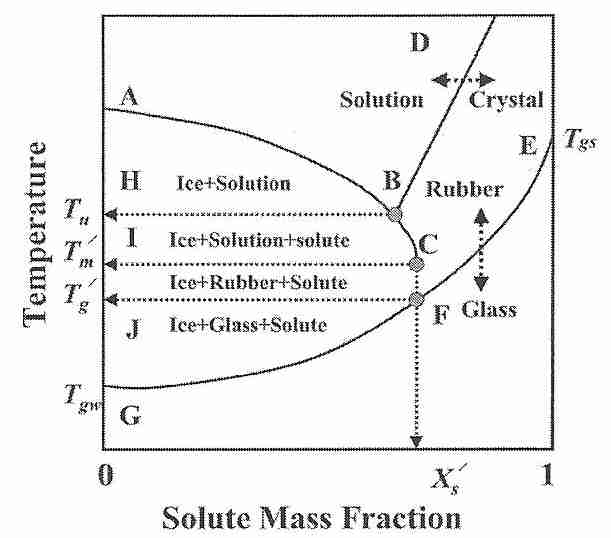 |
Si se enfría a una velocidad de unos 3 millones de ºC por segundo, el agua pura vitrificará a una temperatura de unos −135 ºC ( T gw ). Una solución crioprotectora que vitrificará a una concentración mínima a una temperatura Tgs también vitrificará a una concentración más alta a una temperatura más alta (también llamada Tgs ) . Si parte de la solución de vitrificación se congela por alguna razón, la eliminación del hielo (agua) hará que la mezcla de vitrificación restante esté más concentrada. La temperatura más baja a la que puede producirse la congelación depende de la concentración: una concentración eutéctica se congelará a la temperatura eutéctica ( T u). [Para obtener más información sobre la concentración eutéctica, consulte Solidificación de mezclas eutécticas ]. La temperatura más baja a la que puede ocurrir la congelación en una porción no congelada (solución) es la temperatura de fusión Tm ' .
La temperatura de transición vítrea de la porción descongelada concentrada se denomina Tg ' . Si se forma hielo en una mezcla destinada a vitrificar, como en un paciente de criónica con perfusión imperfecta, la mezcla de vitrificación que queda en la porción no congelada tendrá una concentración más alta y, por lo tanto, una T g más alta (que será T g ' ) [ Figura 1; CRIOBIOLOGIA; Guau, B; 60(1):11-22 (2010)]. 57(1):43-48 (2009) ]. Un significado práctico de este hecho es que si un paciente de criónica se vitrifica parcialmente a una T g ' que está significativamente por encima de la T g esperada, el agrietamiento debido a la tensión térmica puede ocurrir si el enfriamiento no se ralentiza a esa T g ' más alta y no hay cambios en la expansión térmica. [Para una discusión más detallada de T g ' , consulte Algunas propiedades del vidrio .]
El bórax puede aumentar la T g ' al entrecruzarse con solutos y, por lo tanto, aumentar el peso molecular efectivo [ BOLETÍN QUÍMICO Y FARMACÉUTICO; IzutsuK; 51(6):663-666 (2003) ]. Si el bórax puede elevar la Tg de manera similar y reducir la expansión térmica de las muestras vitrificadas, podría reducir el agrietamiento a baja temperatura. Pero, ¿el entrecruzamiento comprometería la información estructural crítica más que el agrietamiento que redujo?
Los estudios piloto realizados en tejidos a temperaturas criogénicas (sin crioprotector) demostraron que el tejido renal tiene más del doble del módulo de elasticidad y cuatro veces la fuerza del tejido cerebral [ CRYOBIOLOGY 33(4):472-482 (1996) y CRYOBIOLOGY 34(4) ):394-405 (1997) ]. Otro estudio piloto mostró una reducción de la expansión térmica con glicerol y DMSO [JOURNAL OF BIOMECHANICAL ENGINEERING 120(2):259-266 (1998)].
VIII. PROTOCOLO DE ENFRIAMIENTO CERCA DE Tg PARA PACIENTES CON CRIONICS VITRIFICANTES
El enfriamiento de los pacientes de criónica a la temperatura del nitrógeno líquido se realiza en una caja de enfriamiento controlada por computadora . Las sondas de temperatura (termopares) se utilizan para monitorear la temperatura del gas en la caja de enfriamiento, en el tórax del paciente, debajo de la piel del cráneo o en la profundidad de la nasofaringe (es decir, en la profundidad de la nariz hasta la parte superior de la garganta) . Una sonda en el tórax proporciona la temperatura corporal central, mientras que la sonda nasofaríngea proporciona una buena representación de la temperatura cerebral central. (No queremos dañar el cerebro introduciendo una sonda en el centro del cerebro).
Un termopar controlará la velocidad de enfriamiento al controlar la velocidad y la duración de la apertura de la válvula que libera nitrógeno líquido en la caja de enfriamiento. Los otros termopares simplemente monitorean la temperatura. La vaporización del nitrógeno líquido es un proceso endotérmico (absorción de calor, impulsado por la entropía) que contribuye significativamente al efecto de enfriamiento.
Para una buena vitrificación , es importante enfriar lo más rápido posible a Tg (supuestamente alrededor de -123 ºC) después de que se complete la perfusión. El enfriamiento rápido reduce el tiempo de exposición a la toxicidad de los crioprotectores y asegura una tasa de enfriamiento por encima de la tasa de enfriamiento crítica , superenfriando al paciente vitrificado y evitando la desvitrificación .
En la fase de enfriamiento inicial, la válvula de control de nitrógeno líquido en la caja de enfriamiento estará esencialmente abierta todo el tiempo sin importar qué termopar se use como termopar de control. Pero a medida que se acerca la Tg, los termopares profundos pueden causar un exceso de temperatura grave a una temperatura excesivamente baja para tejidos menos profundos. La temperatura central del cerebro y (especialmente) del cuerpo cae mucho más lentamente que las temperaturas superficiales debido al tiempo de conducción requerido para que la temperatura más baja vaya de la superficie al centro. Por esta razón, si se usa una temperatura central (o una más cercana al centro, como el cuello o la parte inferior de la garganta) para el termopar de control, los tejidos más superficiales se enfriarán excesivamente. Esto es particularmente cierto inicialmente cuando el enfriamiento es más rápido. Por otra parte,
El termopar de control debe enfriarse justo por encima de Tg. Aunque la tasa de nucleación es muy alta justo por encima de la Tg, la tasa de crecimiento de los cristales es muy baja. Por lo tanto, es seguro sostener a un paciente de criónica vitrificada justo por encima de la Tg, cuando la perfusión del paciente es completa. (Para los pacientes que tienen una perfusión deficiente debido a isquemia, edema o accidente cerebrovascular/aterosclerosis, puede ser mejor bajar rápidamente por debajo de la Tg y correr el riesgo de un mayor agrietamiento que permanecer cerca de la Tg y correr el riesgo de congelarse). Es importante que haya un gradiente de temperatura mínimo en el la cabeza del paciente cuando se enfría por debajo de la Tg porque la falta de una temperatura uniforme es la principal causa del estrés térmico que conduce al agrietamiento por debajo de la Tg.
La Tg de los crioprotectores utilizados en criónica es de unos −123ºC. Aunque la solidificación (vidrificación) de un cerebro humano vitrificado no se produce hasta que la temperatura cae por debajo de -123 ºC, la viscosidad es tan alta a temperaturas más altas que se puede lograr un gran alivio del estrés manteniéndolo a temperaturas muy por encima de la Tg. Por lo tanto, se puede aliviar considerablemente el estrés manteniendo a un paciente con un cerebro vitrificado a −100 ºC, a −110 ºC y a −120 ºC durante períodos de 24 horas. Según se informa, un paciente mantenido a -110 ºC durante tres meses no mostró agrietamiento hasta casi -140 ºC, mientras que un paciente mantenido a -110 ºC durante solo un mes se agrietó a una temperatura mucho más alta.
Después del último de los tres pasos de mantenimiento, a -120 °C, el ser humano podría calentarse a -118 °C en 30 minutos y luego mantenerse a -118 °C durante 2 horas como medio de recocido , no solo aumentando el alivio del estrés a través de una mayor difusión a mayor temperatura. temperatura, pero permitiendo que la temperatura de la superficie se acerque a la temperatura central (una mayor uniformidad de la temperatura da como resultado una menor tensión térmica).
Los experimentos con concentraciones vitrificables de propilenglicol crioprotector (T g , −108 ºC) han demostrado que incluso un enfriamiento muy lento y uniforme de una muestra de 482 ml no puede evitar la fractura a temperaturas inferiores a 25 ºC por debajo de T g (−132 ºC) [CRIOBIOLOGÍA; Fahy, GM; 27(5):492-510 (1990)]. y seguramente habría mucho más daño acercándose a la temperatura del nitrógeno líquido (−196ºC). No obstante, tanto un riñón de conejo como un hemicerebro de conejo se han enfriado a la temperatura del nitrógeno líquido sin agrietarse utilizando soluciones de vitrificación más nuevas. Este resultado no se puede esperar de muestras más grandes. Las muestras de mayor volumen se fracturan a temperaturas más altas que las muestras de pequeño volumen cuando la velocidad de enfriamiento es la misma [Tabla 2; CRIOBIOLOGIA; Fahy, GM; 27(5):492-510 (1990)].
Cada metal tiene una velocidad de enfriamiento por encima de la cual pueden ocurrir tensiones que conducen al agrietamiento, mientras que las velocidades de enfriamiento más lentas no conducen al agrietamiento. No hay ninguna razón por la que los materiales de vidrio o cerámica deban ser diferentes, y los órganos vitrificados son razonablemente uniformes. La diferencia crítica radica en el hecho de que los metales e incluso los vidrios no biológicos se unen mediante enlaces más fuertes (generalmente covalentes) que los que se encuentran en los vidrios formados por crioprotectores biológicamente vitrificantes. Los enlaces de hidrógeno se rompen más fácilmente, lo que significa que para evitar las tensiones térmicas que conducen al agrietamiento en un paciente de criónica que se enfría a la temperatura del nitrógeno líquido, puede ser necesario enfriar a velocidades del orden de unas pocas milésimas de grado por hora, no una velocidad de enfriamiento que se puede lograr por cualquier medio práctico.
Debido a que el agrietamiento es inevitable al enfriar un cerebro humano vitrificado a la temperatura del nitrógeno líquido, es mejor inducir el agrietamiento a temperaturas más altas. Las grietas inducidas a temperaturas más altas son menos y más anchas, mientras que si las grietas no ocurren hasta temperaturas más bajas, las grietas resultantes serán extremadamente pequeñas y numerosas [Figura 8; CRIOBIOLOGIA; Fahy, GM; 27(5):492-510 (1990)], que es más dañino. Por lo tanto, el próximo paso en el protocolo de enfriamiento es enfriar algo rápido (alrededor de 1 ºC por minuto) a -145 ºC para inducir el agrietamiento a mayor temperatura.
La fracturación a temperaturas más altas reduce, pero no elimina, la posibilidad de fracturarse a temperaturas más bajas. Después del paso de inducción de grietas, el enfriamiento exponencial en lugar de lineal a -196 ºC es el mejor medio para reducir las grietas debido al estrés térmico. La expansividad térmica disminuye a medida que disminuye la temperatura (se produce una disminución precipitada de la expansividad térmica en T g ), pero el tiempo de relajación (tiempo para que las tensiones se alivie en su mayoría) aumenta aún más que la expansión térmica disminuye a medida que la temperatura desciende por debajo de T g . Además, la conductividad térmicadisminuye con la disminución de la temperatura (que ya es muy baja para materiales no metálicos no cristalinos). Como resultado, el estrés térmico aumenta a un ritmo cada vez mayor por cada grado de enfriamiento por debajo de Tg . Por lo tanto, la disminución de la velocidad de enfriamiento a medida que baja la temperatura da como resultado un menor estrés térmico que el enfriamiento a una velocidad constante por debajo de Tg .
Todo el protocolo de enfriamiento humano, incluido el enfriamiento exponencial por debajo de −145ºC, podría ser algo como:
enfriar lo más rápido posible a −100ºC mantener a −100ºC durante 24 horas (alivio del
estrés)
enfriar de −100ºC a −110ºC en 1 hora (10ºC/hora)
mantener a −110ºC durante 24 horas (alivio del estrés)
enfriar de −110ºC a −120 ºC en 1 hora (10 ºC/hora)
mantener a −120 ºC durante 24 horas (alivio de tensión)
calentar de −120 ºC a −118 ºC en 1 hora (recocido)
mantener a −118 ºC durante 2 horas (recocido)
enfriar de −118 ºC a − 145ºC en 30 minutos (paso de craqueo con enfriamiento rápido)
enfriar de -145ºC a -170ºC en 25 horas (1ºC/hora)
enfriar de -170ºC a -190ºC en 50 horas (0,4ºC/hora)
enfriar de -190ºC a -196ºC en 24 horas (0,25ºC/hora)
VIII. ALMACENAMIENTO POR ENCIMA DE LA TEMPERATURA DEL NITRÓGENO LÍQUIDO
Para los pacientes de criónica que no están vitrificados, pero para quienes las mezclas de crioprotector/agua congelan temperaturas considerablemente superiores a la Tg , habrá una tensión interna considerable muy por encima de la Tg . Un enfriamiento más rápido de estos pacientes puede reducir la cantidad de congelación y el tamaño de los cristales de hielo, pero aumentar la cantidad de hielo intracelular y el tamaño de las grietas. Aunque un enfriamiento lo suficientemente lento teóricamente podría eliminar el agrietamiento, incluso con un enfriamiento muy lento, el riesgo de agrietamiento se vuelve significativo alrededor de −20ºC por debajo de T g. (Ya sea para congelación o vitrificación, la cantidad de estrés interno creado aumentará con el tamaño del paciente de criónica). Se requerirá tecnología molecular futura para reparar tanto el agrietamiento como la congelación, y es difícil saber qué mezcla de agrietamiento y la congelación será óptima para una tecnología que todavía es especulativa. Sin vitrificación, el almacenamiento a temperatura de nitrógeno líquido parece más prudente, porque esa temperatura permitirá la mejor conservación durante la larga espera para que se desarrolle la tecnología requerida. El almacenamiento a temperatura de nitrógeno líquido sería menos vulnerable al daño por radiación que el almacenamiento a temperatura criogénica más alta. (Vea mi ensayo Daño por radiación a temperatura criogénica ).
Basándose en la suposición de que el almacenamiento a largo plazo de pacientes de criónica vitrificada necesariamente debe estar cerca de T g para evitar grietas o fracturas, los ingenieros del proyecto Timeship han diseñado unidades de crioalmacenamiento que pueden mantener las temperaturas más altas de manera económica y robusta. Cuando y si el almacenamiento de Timeship esté disponible, se anticipa que estará abierto a miembros de cualquier organización de criónica. La organización de criónica Alcor tiene almacenamiento de temperatura criogénica intermedia disponible para algunos pacientes neurológicos, pero a un costo mucho más alto que el almacenamiento de nitrógeno líquido.
(Para algunas especulaciones sobre la movilidad molecular a temperaturas criogénicas, consulte mi ensayo Molecular Mobility at Low Temperature ).
 diciembre 16, 2022
diciembre 16, 2022

